光增强固定于MXene纳米片上的溶菌酶活性,用于耐甲氧西林金黄色葡萄球菌(MRSA)的杀菌应用
耐药细菌已成为全球日益严重的公共卫生问题。其中,耐甲氧西林金黄色葡萄球菌(MRSA)可导致软组织感染、菌血症和其他致命疾病,并伴有高发病率和死亡率。现有的抗菌方法仍然存在着容易导致新的耐药性的产生、材料合成繁琐、纯化难度大和成本高等问题,急需开发出一种安全、高效、低成本的抗菌药物。生物体内的溶菌酶能够催化肽聚糖中N-乙酰胞壁酸和N-乙酰-D-氨基葡萄糖残基之间的β-1,4-键的水解,从而表现出抗菌能力。溶菌酶具有极高的生物安全性,人们将其作为抗菌剂广泛地应用于食品工业。然而,溶菌酶的稳定性有限、可重复使用性差和不可控性一直阻碍着它的应用。酶的固定化不仅不会破坏酶的结构,还可以提高酶的可重复使用性和催化活性。此外,具有光热转换效应的纳米结构作为功能载体,能够同时实现酶的固定和酶活性的光热控制,使远程控制生物催化反应成为可能。然而,这种策略还没有在溶菌酶的抗菌应用中进行过探索。
本文构建了一个基于MXene生物界面工程的光热纳米抗菌材料,通过激光对溶菌酶的活性进行调控,从而有效杀灭MRSA。如图1所示,单层Ti3C2 MXene通过聚多巴胺(PDA)表面化学进行功能化,以增强光热效应和稳定性,在此过程中溶菌酶通过分子间静电亲和力固定在这种二维杂化界面上。合成的纳米材料(记为M@P@Lyso)光热转换效率可达到46.88%,在实现溶菌酶的固定化的同时,通过激光调控使局部温度升高,激活溶菌酶的杀菌活性。体外和体内抗菌实验表明,M@P@Lyso能有效抑制MRSA的增殖,加速小鼠伤口消毒,同时具有可忽略的细胞毒性和优异的生物相容性。M@P@Lyso突出的抗菌活性应归因于多重杀菌机制的协同作用,即光热促进溶菌酶生物催化活性、M@PDA产生的局部过热效应以及纳米片的物理切割效应。该研究提出了一种简单地通过控制激光照射来增强溶菌酶杀菌作用的方法,有希望用于治疗多重耐药细菌感染,为研发高稳定性、高活性抗菌纳米复合物及推广应用提供了技术参考。
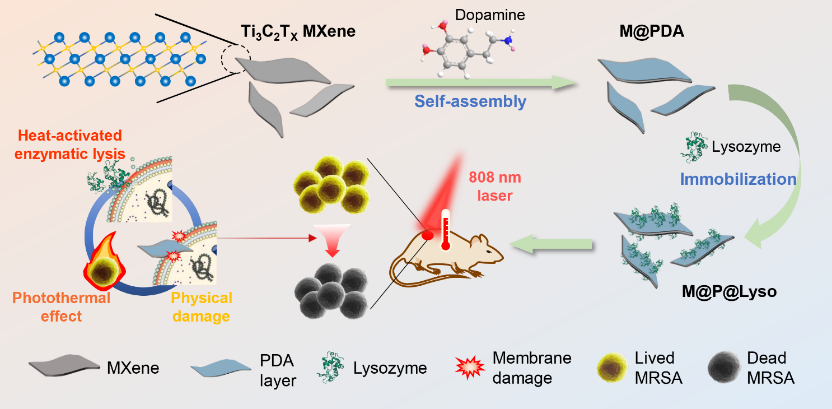
溶菌酶在MXene上的生物界面工程化及光热增强下对MRSA杀菌示意图
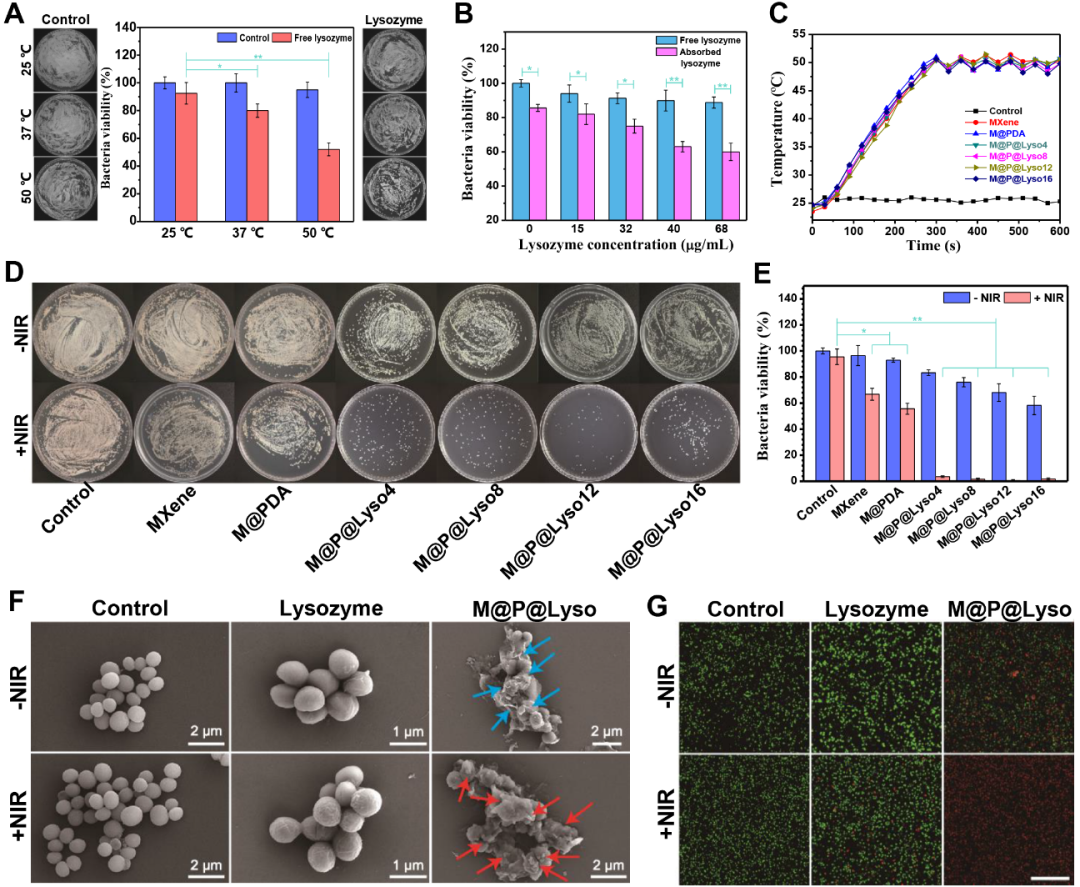
合成的M@P@Lyso具有优异的光热转换性能,光热转换效率达到46.88%。经过5个循环后,M@P@Lyso12依然有着稳定的光热转换能力,为光热调控溶菌酶活性从而实现更强杀菌效力的设想提供了基础。

溶菌酶对MRSA的杀菌效果具有浓度依赖性,且局部温度升高和固定化均对溶菌酶的杀菌效果有积极作用。M@P@Lyso+NIR可以有效杀灭MRSA,仅经过10 min的激光处理,40 μg/mL的M@P@Lyso可以达到>95%的杀菌率。M@P@Lyso+NIR的抗菌活性应归因于多重杀菌机制的协同作用:光热作用产生的局部温度升高使得溶菌酶的水解活性得到极大的增强,由光热产生的局部过热效应以及纳米片的物理切割效应共同起作用,破坏细菌细胞,实现高效杀菌。
参考文献
Zhang, D., Huang, L., Sun, D.-W., Pu, H., & Wei, Q. (2022). Bio-interface Engineering of MXene Nanosheets with Immobilized Lysozyme for Light Enhanced Enzymatic Inactivation of Methicillin-Resistant Staphylococcus aureus. Chemical Engineering Journal, 139078.
https://doi.org/10.1016/j.cej.2022.139078
1、凡本网所有原始/编译文章及图片、图表的版权均属微生物安全与健康网所有,未经授权,禁止转载,如需转载,请联系取得授权后转载。
2、凡本网未注明"信息来源:(微生物安全与健康网)"的信息,均来源于网络,转载的目的在于传递更多的信息,仅供网友学习参考使用并不代表本网同意观点和对真实性负责,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请速来函告知,我们将尽快处理。
3、转载请注明:文章转载自www.mbiosh.com
联系方式:020-87680942

