意想不到的小帮手:微生物群刺激系统性抗病毒防御
微生物群的先天免疫激活是由一组专用的、种系编码的先天免疫传感器介导,即所谓的模式识别受体。打破肠道上皮屏障的微生物通常被toll样受体(Toll-like receptors,TLRs)感知。随后的炎症反应引发局部抗菌免疫反应,但也引起和/或促进疾病的发病机制。最近,Erttmann等[1]人发表在《Immunity》杂志上的一项研究中,不同于TLRs和细菌-细胞直接接触的识别模式,肠道菌群通过I型干扰素(Interferon,IFN)启动并促进低水平的系统性先天免疫激活,从而保护小鼠免受病毒入侵,揭示了一种意想不到的有益作用。
如图所示,含有细菌DNA的膜囊泡(Membrane vesicles,MVs)由肠道内的菌群释放并穿过上皮屏障。在MVs靶向细胞过程中,DNA被环GMP-AMP合酶(cyclic GMP–AMP synthase,cGAS)识别。cGAS激活后,产生2’–3’连锁环GTP-ATP(2’–3’ linked cyclic GTP-ATP,cGAMP)。反过来,cGAMP结合到干扰素基因的刺激因子(Stimulator of interferon genes,STING)上,使其寡聚,并从内质网(Endoplasmic reticulum,ER)运输到高尔基体。STING的激活最终导致I型IFN和其他促炎细胞因子的转录上调和分泌。分泌的IFN以自分泌或旁分泌的方式与细胞结合,诱导数百个IFN刺激基因(ISGs)的转录,使细胞进入抗病毒状态。
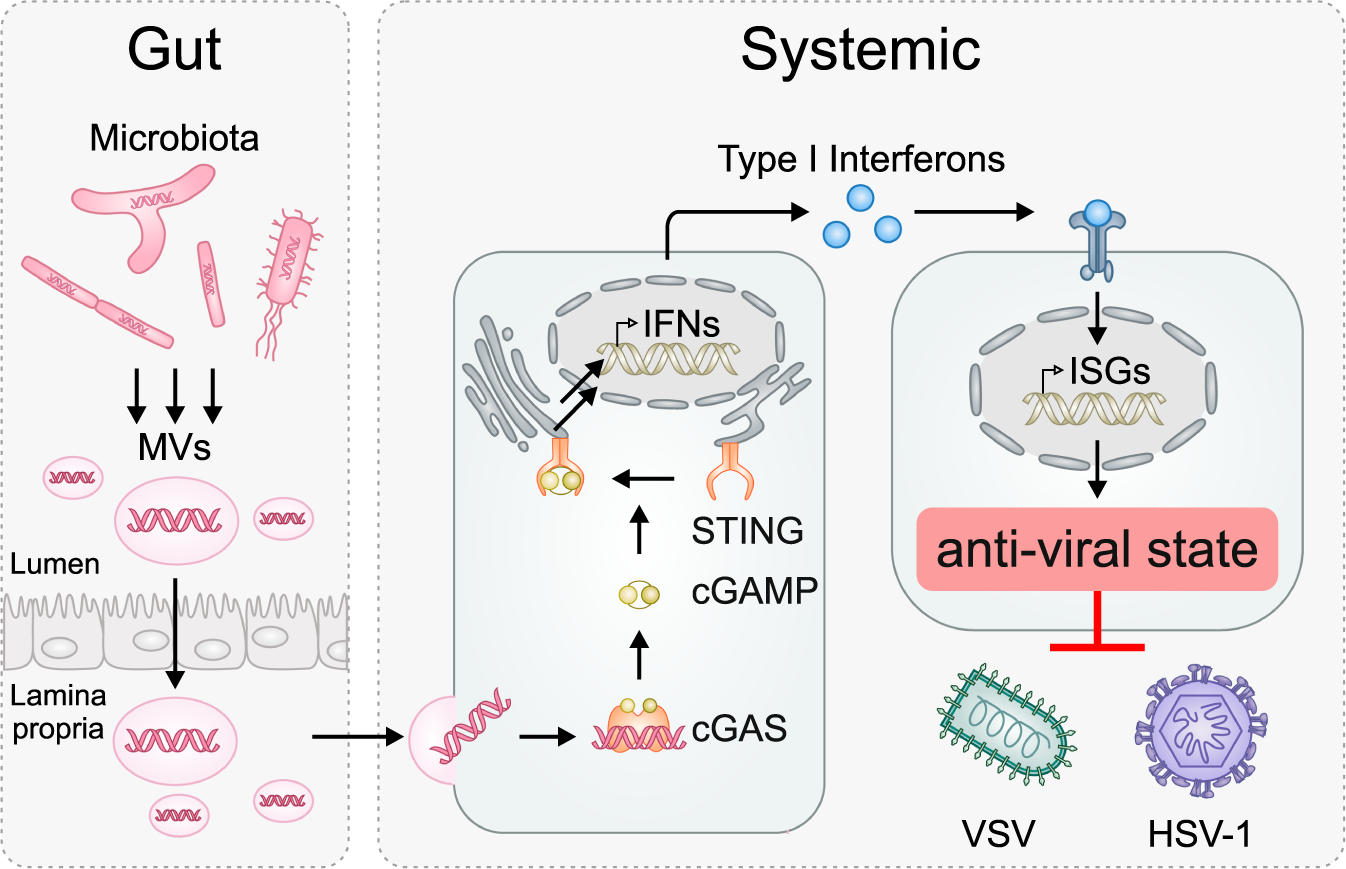
肠道菌群通过cGAS-STING轴启动I型IFN反应,促进低水平的系统性先天免疫激活,从而保护局部和远端宿主细胞免受病毒威胁的分子机制[2]。
总之,Erttmann等人的研究证明了微生物群通过cGAS-STING轴启动全身I型IFN反应的作用,从而保护局部和远端宿主细胞免受外部威胁:病毒。微生物群促进抗病毒免疫的机制得到了实验验证,强调了共生源性MVs是微生物群和先天免疫系统之间的系统交流平台,突出了共生细菌和寄主之间互利关系的新机制。
参考文献:
[1] https://doi.org/10.1016/j.immuni.2022.04.006.
[2] https://doi.org/10.1038/s41392-022-01217-2.
1、凡本网所有原始/编译文章及图片、图表的版权均属微生物安全与健康网所有,未经授权,禁止转载,如需转载,请联系取得授权后转载。
2、凡本网未注明"信息来源:(微生物安全与健康网)"的信息,均来源于网络,转载的目的在于传递更多的信息,仅供网友学习参考使用并不代表本网同意观点和对真实性负责,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请速来函告知,我们将尽快处理。
3、转载请注明:文章转载自www.mbiosh.com
联系方式:020-87680942

