YY2/DRP1信号通路通过抑制线粒体分裂破坏肿瘤干细胞不对称分裂
肿瘤干细胞(CSCs)与肿瘤的发生、进展、复发和治疗耐药性有关。为了在促进肿瘤发生的同时维持它们的细胞池,CSCs发生不对称地裂,产生CSC和高度增殖,更分化的转运扩增细胞。耗尽CSC池被认为是一种有效的抗肿瘤策略;然而,人们对CSC分裂的机制仍然知之甚少,因此在很大程度上限制了其临床应用。
近日,重庆大学吴寿荣教授和江启慧(Vivi Kasim)教授团队在国际权威学术期刊《Advanced Science》上在线发表题为“YY2-DRP1 Axis Regulates Mitochondrial Fission and Determines Cancer Stem Cell Asymmetric Division”的原创性研究论文。本研究发现YY2/DRP1信号通路可以通过抑制线粒体的分裂,破坏肿瘤干细胞的不对称分裂,诱发肿瘤干细胞池的枯竭,从而抑制肿瘤的起始能力和肿瘤的发生发展。

最近的研究揭示了CSCs不对称分裂的调节过程,包括细胞周期的进展,这与自我更新,肿瘤发生和耐药性有关。另一种机制涉及线粒体裂变和不对称分离,即年轻、健康的线粒体产生并不对称地分布到两个子细胞中。因此,接受到较少相对功能失调的线粒体(以下简称“功能失调线粒体”)的细胞保持其干性;而接受较少相对“健康”线粒体(以下简称“健康”线粒体)的细胞则失去其干性。然而,CSC不对称分裂的调节机制仍然知之甚少,限制了治疗应用。
转录因子在调节各种途径(包括发育和分化)中起着关键作用。许多指导发育决策的转录因子的异常表达可以通过促进肿瘤的发生、进展和转移来增加其致癌性。毫不奇怪,转录因子稳态对于CSC维持至关重要。这种平衡的破坏会导致各种干性相关基因的表达发生变化。尽管转录因子在维持CSC池方面很重要,但转录因子在CSC不对称分裂中的作用尚不清楚。
在本研究中,我们鉴定了YY2,一种属于阴阳家族的活化或抑制性锌指转录因子,作为CSC的新型负调节剂。我们表明YY2损害不对称干细胞分裂并促进肝脏CSCs产生更多分化的后代,从而抑制CSCs的肿瘤起始能力和肿瘤发生。考虑到YY2在临床HCC病变以及其他癌症中下调,YY2下调与肝癌患者疾病进展和预后不良相关,这些结果表明一种新的YY2依赖性调节机制作用于CSCs,以及药理学靶向CSCs不对称分裂的新治疗机会。
为了进一步阐明YY2是如何影响线粒体分裂,进而抑制肿瘤干细胞的自我更新功能,该研究考察了YY2对线粒体分裂因子表达的影响。结果显示YY2能结合DRP1的启动子从而显著抑制其转录活性,导致干细胞样细胞中线粒体分裂因子DRP1和线粒体分裂水平降低,破坏线粒体的动态平衡。该研究通过各种体内外实验证明YY2/DRP1通路通过抑制线粒体分裂,诱发损伤线粒体的产生从而破坏肿瘤干细胞不对称分裂并促进肿瘤干细胞的分化,引发肿瘤干细胞池的枯竭,最终抑制肿瘤的起始能力和肿瘤的发生发展。
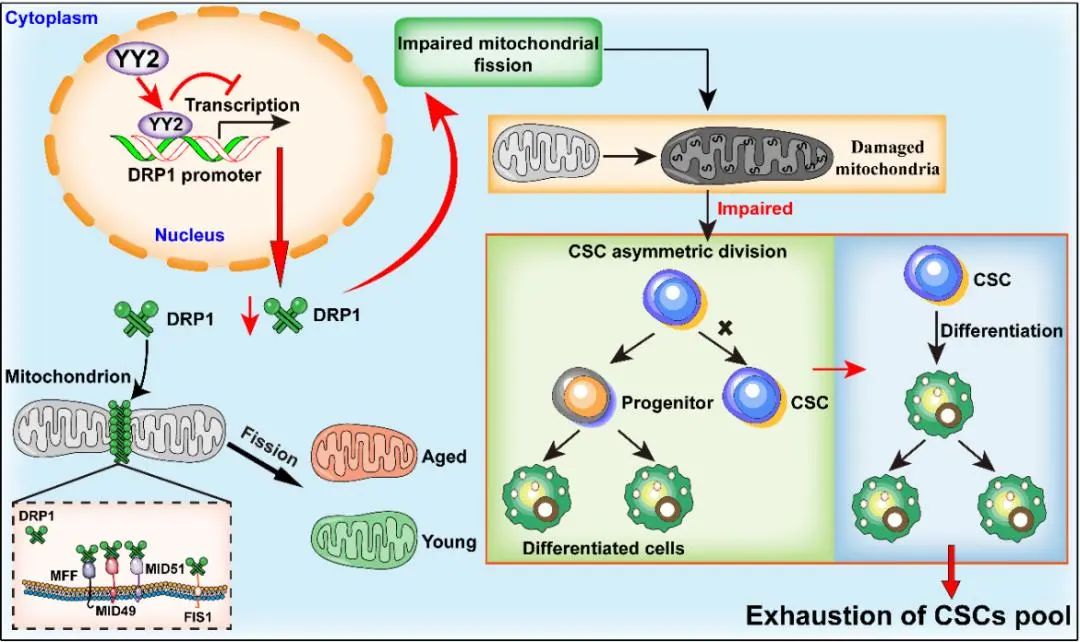
YY2/DRP1信号通路通过抑制线粒体分裂破坏肿瘤干细胞不对称分裂。
综上所述,虽然需要进一步的研究来证实YY2 / DRP1轴在调节HCC以外的肿瘤中CSC的作用,但在本研究中,我们将YY2确定为CSC不对称分裂的新型调节因子,并将其与DRP1介导的线粒体裂变联系起来。此外,我们提供了强有力的证据表明,促进CSC分化和CSC池耗尽的YY2过表达可以使CSC对DNA损伤诱导剂敏感。因此,我们的研究结果不仅突出了YY2、线粒体裂变与CSC自我更新之间前所未有的关系,而且为CSCs线粒体裂变的调控机制以及YY2肿瘤抑制作用的分子途径提供了新的见解。最后,我们的研究指出YY2是肝癌的新型治疗靶点。
参考资料:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202207349
1、凡本网所有原始/编译文章及图片、图表的版权均属微生物安全与健康网所有,未经授权,禁止转载,如需转载,请联系取得授权后转载。
2、凡本网未注明"信息来源:(微生物安全与健康网)"的信息,均来源于网络,转载的目的在于传递更多的信息,仅供网友学习参考使用并不代表本网同意观点和对真实性负责,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请速来函告知,我们将尽快处理。
3、转载请注明:文章转载自www.mbiosh.com
联系方式:020-87680942

