线粒体功能障碍与眼表炎症发生发展的联系
角膜上皮细胞位于眼表的最外层,与周围环境直接接触。长期暴露于低湿度、高风速、蓝光和药物防腐剂等应激环境中,会导致泪膜不稳定,引起高渗透压,从而损伤上皮细胞并引发炎症反应,最终导致眼表疾病的发生。眼表炎症是由固有免疫系统产生的上皮细胞应激的标志。然而,在各种环境应激下眼表上皮细胞是否启动固有免疫以及如何启动固有免疫的机制尚不清楚。深入研究这个问题将有助于更好地理解眼表的免疫环境,并对眼表炎症的治疗提供指导。
近日,厦门大学眼科研究所在Signal Transduction and Targeted Therapy杂志发表题为“The cGAS-STING pathway-dependent sensing of mitochondrial DNA mediates ocular surface inflammation”的研究论文。该研究发现,多种外界刺激可以导致角膜上皮细胞线粒体功能障碍和线粒体膜通透性转换孔(mPTP)的开放,使得线粒体DNA(mtDNA)泄漏进入胞质中,进而激活cGAS-STING信号通路从而介导眼表炎症。

该研究采用苯扎氯氨毒性眼表损伤以及泪腺摘除诱导干眼等动物模型,建立不同因素诱导的眼表炎症模型。研究人员观察到cGAS-STING信号通路的激活与眼表炎症之间存在明显的相关性。苯扎氯氨处理的小鼠以及泪腺摘除小鼠角膜荧光素染色增加,结膜杯状细胞丢失,伴随着cGAS、STING表达的上调。研究人员进一步分析了干眼患者和正常受试者提取的泪液蛋白,结果也支持了这些发现,发现干眼患者中cGAS和STING水平升高。此外,研究人员还发现STING蛋白水平与角膜荧光素染色评分呈正相关,而与水性泪液分泌呈负相关。
为了验证cGAS-STING信号通路在眼表炎症中的作用,研究人员构建了STING基因敲除(STING-/-)小鼠。有趣的是,STING的缺失显著减轻了角膜荧光素染色和眼表上皮细胞的损伤,同时伴随着炎症因子水平的降低。此外,研究人员探索了STING抑制剂C-176在眼表炎症治疗中的潜力,发现C-176可以抑制STING的激活,改善角膜荧光素染色,并减轻眼表上皮细胞的丢失,这为眼表炎症和角膜上皮损伤的治疗提供了一个非常有前景的新靶点。
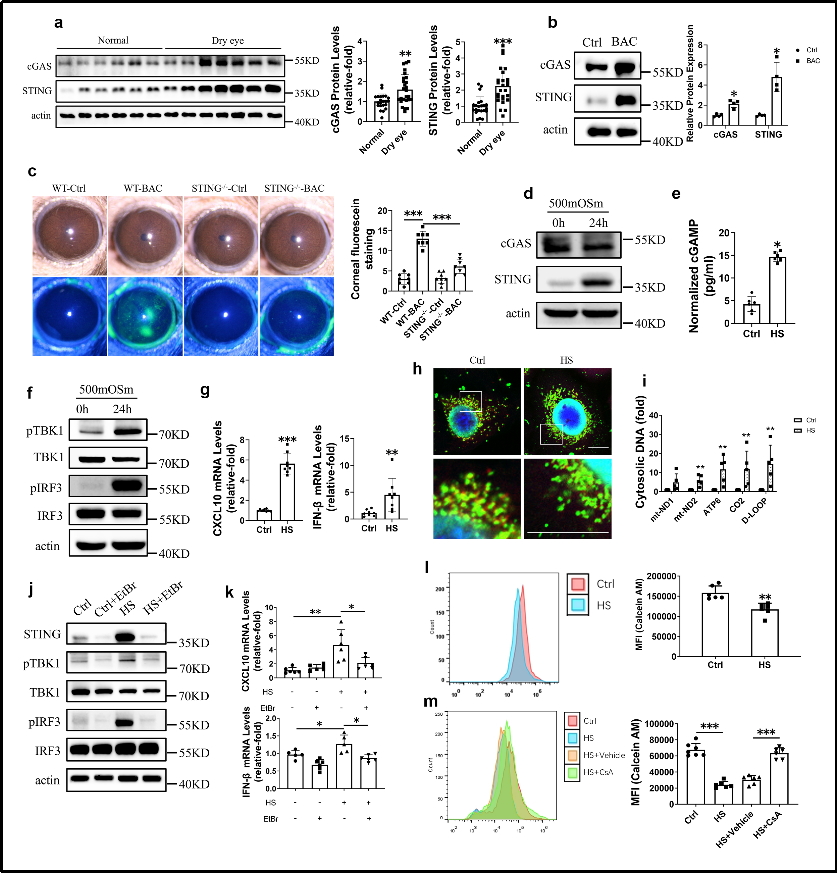
泪液渗透压升高是干眼对眼表炎症和角膜损伤的重要病理机制,为了进一步探索cGAS-STING信号通路在干眼病理生理过程中的作用,研究人员在高渗条件下培养角膜上皮细胞(HCE),发现高渗导致cGAS和STING水平升高,cGAMP的产生,TBK1和IRF3的磷酸化,以及炎症细胞因子的上调。进一步利用小干扰RNA进行的研究证实,敲降cGAS或STING显著减少了HCE中高渗应激引起的炎症反应。此外,研究人员观察到在暴露于高渗应激的HCE中线粒体形态学变化、线粒体钙离子水平增加和线粒体超极化等改变,导致线粒体功能障碍,引起线粒体渗透转换孔(mPTP)开放,随之mtDNA释放到胞质中。使用临床上治疗干眼的药物环孢素(CsA)可以逆转mPTP的开放以及EtBr耗竭胞质内的mtDNA,均能有效降低cGAS-STING通路的激活及下游炎症因子的表达。
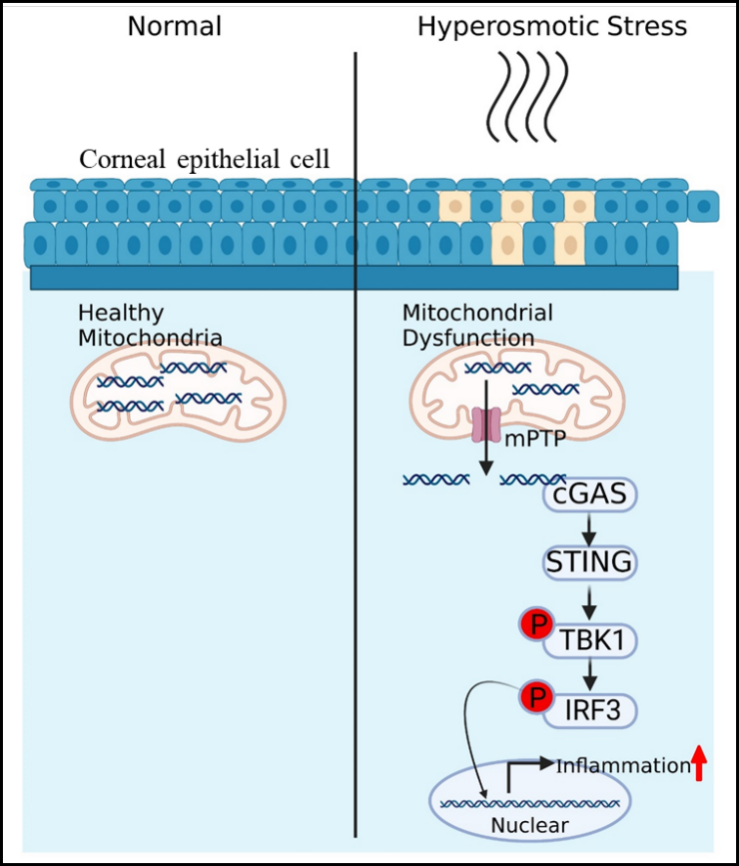
该研究首次发现cGAS-STING信号通路参与眼表炎症的发生发展过程,揭示了线粒体功能障碍与眼表炎症发生发展的联系,为眼表炎症反应的病理生理过程研究提供了新的视角。这些新发现为临床上理解多种眼表应激反应提供了理论依据,并为眼表炎症的治疗提供了新的靶点。
原文链接:https://www.nature.com/articles/s41392-023-01624-z
1、凡本网所有原始/编译文章及图片、图表的版权均属微生物安全与健康网所有,未经授权,禁止转载,如需转载,请联系取得授权后转载。
2、凡本网未注明"信息来源:(微生物安全与健康网)"的信息,均来源于网络,转载的目的在于传递更多的信息,仅供网友学习参考使用并不代表本网同意观点和对真实性负责,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请速来函告知,我们将尽快处理。
3、转载请注明:文章转载自www.mbiosh.com
联系方式:020-87680942

