探秘灵芝提取物——开启肠道健康新 “蘑” 法
探秘灵芝提取物——开启肠道健康新 “蘑” 法


灵芝作为知名的食药用菌,具有多种健康功效,如预防癌症、神经退行性疾病和心血管疾病等。其中,灵芝(Ganoderma lucidum,GL)是被广泛研究的食药用菌,而新日本灵芝(Ganoderma neo-japonicum,GN)的药用潜力尚待深入探索。灵芝富含多种生物活性化合物,如三萜类和多糖,多糖在调节肠道微生物群和影响宿主健康方面起着关键作用。然而,不同灵芝物种提取物对个体肠道微生物群的影响仍未完全明确。
肠道微生物群在人体众多生理过程中发挥着重要作用,参与能量产生、葡萄糖和脂质代谢、免疫调节等。膳食纤维(如多糖)可被肠道细菌分解,影响肠道健康。多糖发酵产生的短链脂肪酸(SCFAs)对维持结肠细胞能量供应、调节免疫反应等具有重要意义。此外,大多数灵芝提取物为粗提物,其多种生物活性化合物可能协同影响肠道微生物群组成。近日,泰国农业大学农业工业学院生物技术系的益生元和益生菌健康专业研究团队Suttipun Keawsompong在《International Journal of Biological Macromolecules》期刊发表题为“Simulated gut microbiota fermentation of polysaccharide extracts from Ganoderma lucidum and Ganoderma neo-japonicum”的文章,首次对比研究GL和GN热水提取物对肠道微生物群的影响。

一、生物活性成分与特征
傅里叶变换红外光谱(FTIR)显示,GL和GN的功能成分相似,但强度不同。GL和GN均富含多糖,两者单糖组成中均含葡萄糖、半乳糖和甘露糖,但比例不同(图1)。FTIR 和 核磁共振(NMR) 分析表明,它们具有相似的功能成分,但强度和结构存在差异,如 GL 含有β- 1,6-Glcp 和α- 4,6 -Glcp 结构,而GN中不存在(图2)。
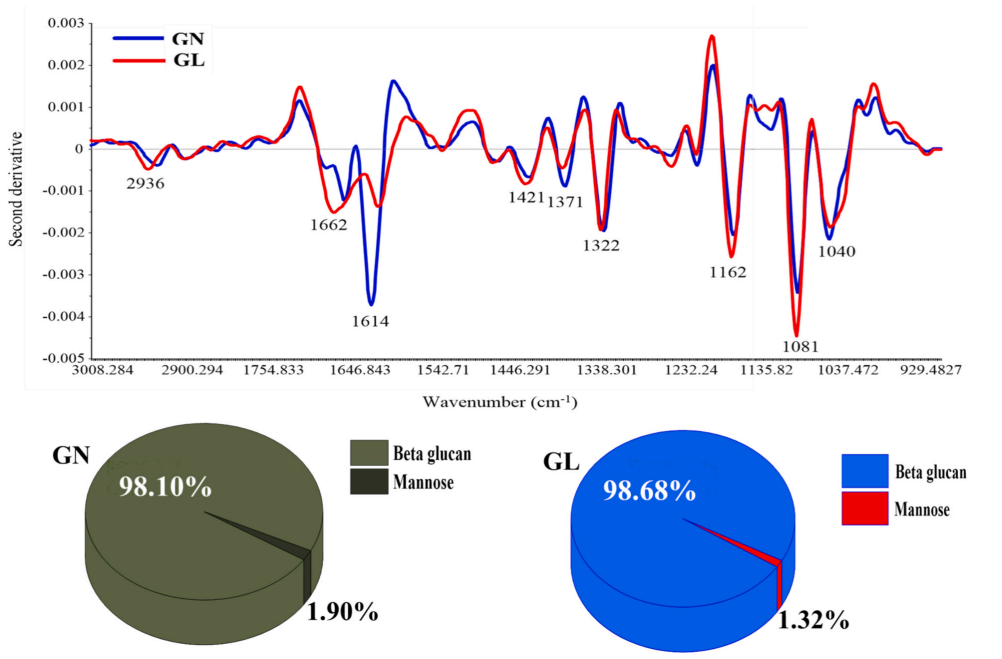
图1 傅里叶变换红外光谱(FTIR)以及甘露糖和β-葡聚糖的百分比(饼状图)
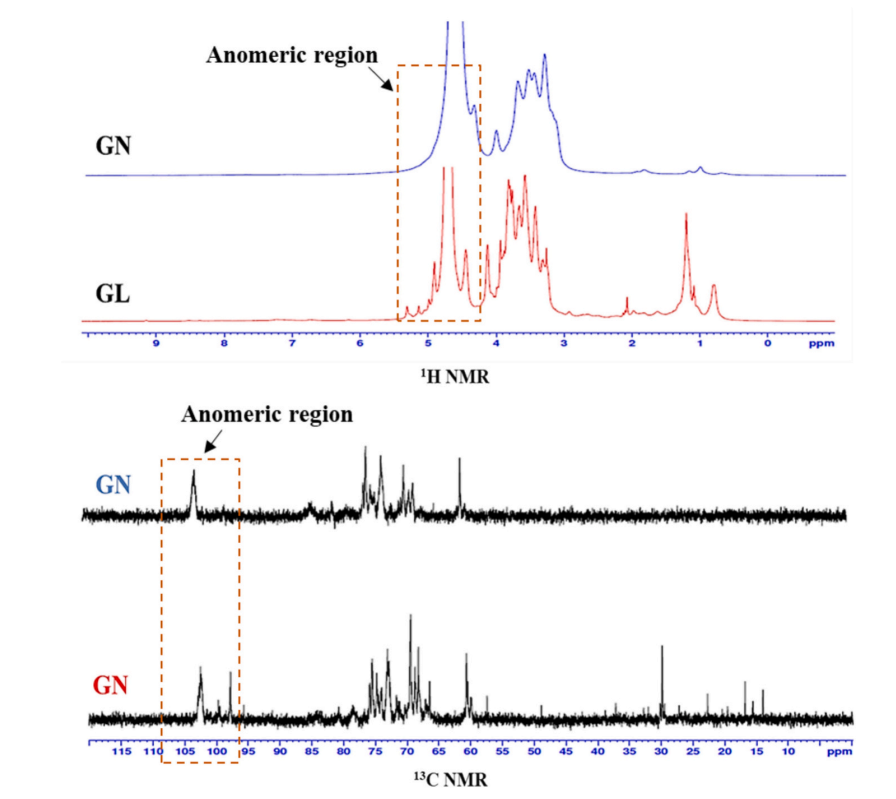
图2 GL和GN核磁共振谱
二、对肠道微生物群的影响
在肠道微生物群发酵后,对34个样本(来自GL、GN和对照发酵,时间从0到24h)进行16S核糖体DNA基因V3-V4区域的双端测序。如表1和图3所示,通过不同指数分析,各实验组微生物群落中未观察到明显的结构变异。如图4所示,发酵后,GL和GN均能改变肠道微生物群组成。GL和GN既能促进有益细菌的生长,又能抑制致病微生物群的增殖。在门水平上,它们抑制了假单胞菌门(Pseudomonadota)的生长,促进了芽孢杆菌门(Bacillota)、拟杆菌门(Bacteroidota)和放线菌门(Actinomycetota)的生长。在纲水平上,抑制了γ -变形菌纲(Gammaproteobacteria)的增殖,促进了梭菌纲(Clostridia)和拟杆菌纲(Bacteroidia)等有益菌的生长。在科水平上,促进了普雷沃氏菌科(Prevotellaceae)、瘤胃球菌科(Ruminococcaceae)等有益菌科的生长,抑制了肠杆菌科(Enterobacteriaceae)的生长,且GL的调节作用更显著(图5、图6)。
表1 通过Chao1、香农和辛普森指数随时间测定的不同批次(B1、B2和B3)对照组、GL组和GN组微生物种群的α多样性
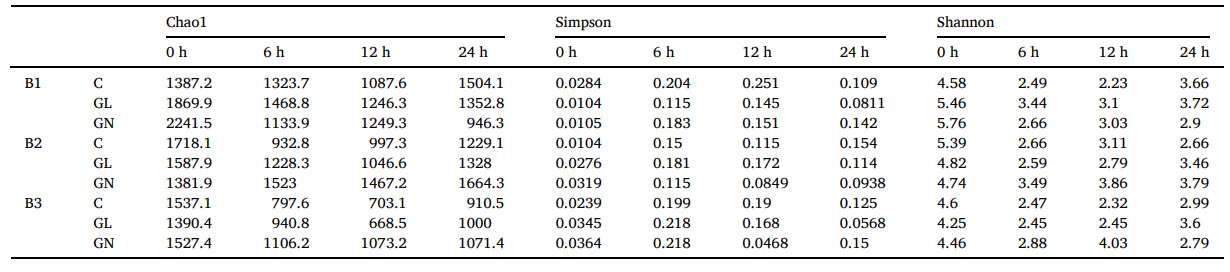
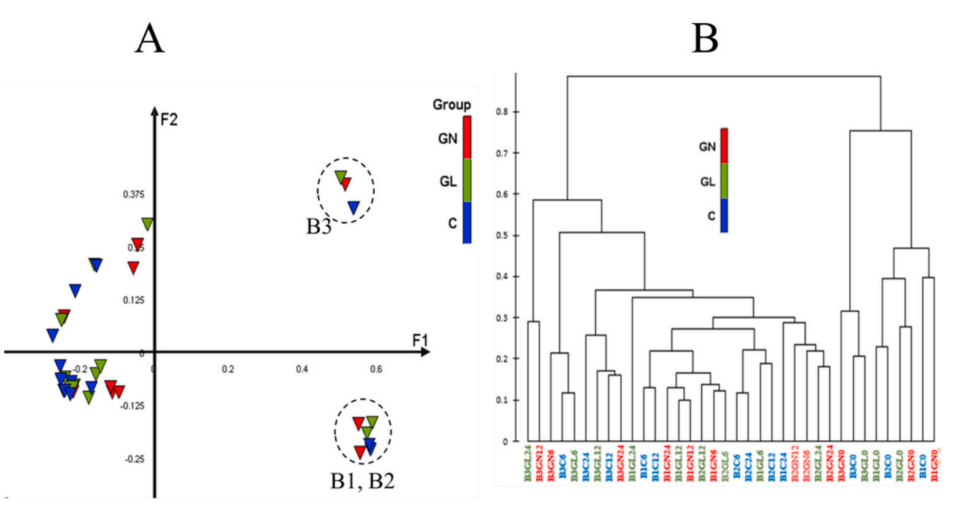
图3 组间微生物种群分析
注:(A)基于ASV水平的Bray-Curtis距离的主坐标分析图;(B)ASV水平的层次聚类树。对照:C,灵芝提取物:GL,新日本灵芝提取物:GN。
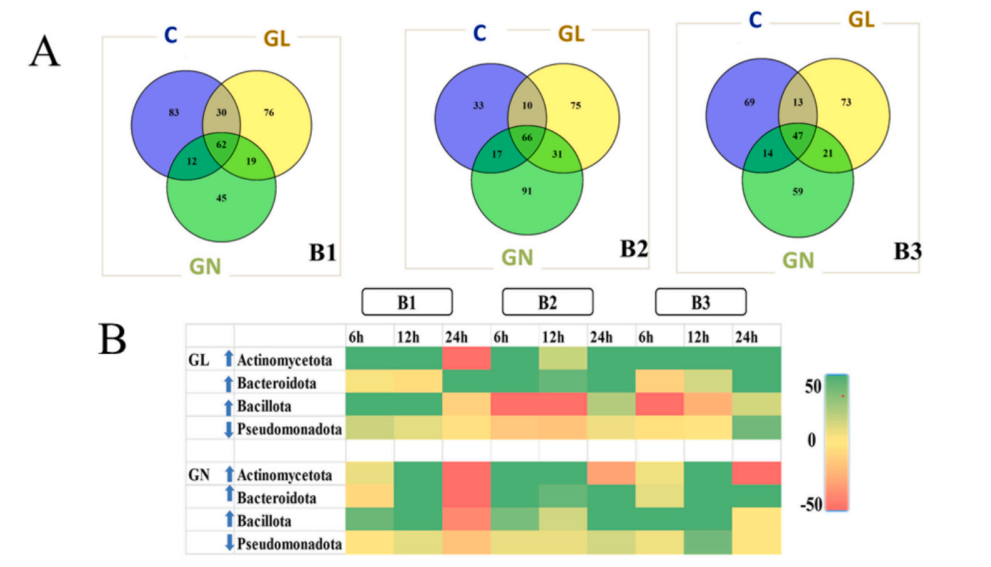
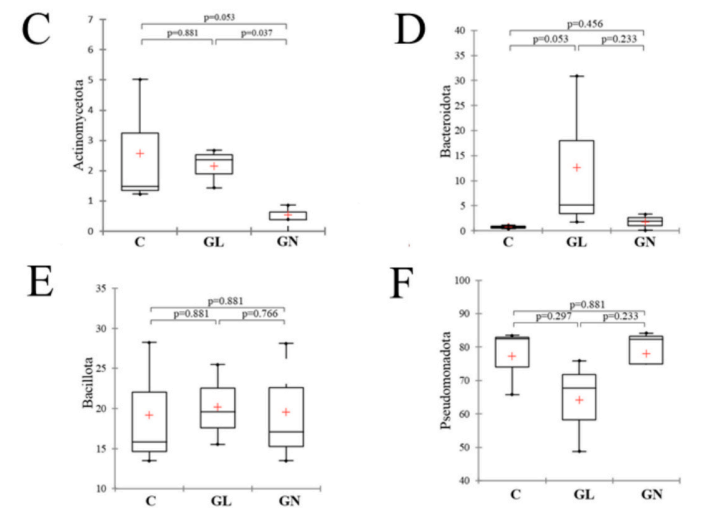
图4 各批次(B1、B2和B3)中各组在门水平上的肠道微生物群比较
注:(A)维恩图展示了不同组之间共享和独特的扩增子序列变异(ASV)。(B)热图描绘了从6小时到24小时GL和GN的影响;绿色代表积极影响,黄色表示中性,红色表示负面影响。放线菌门(C)、拟杆菌门(D)、芽孢杆菌门(E)和假单胞菌门(F)各组之间细菌丰度的成对比较箱线图。对照组:C,灵芝提取物:GL,新日本灵芝提取物:GN。
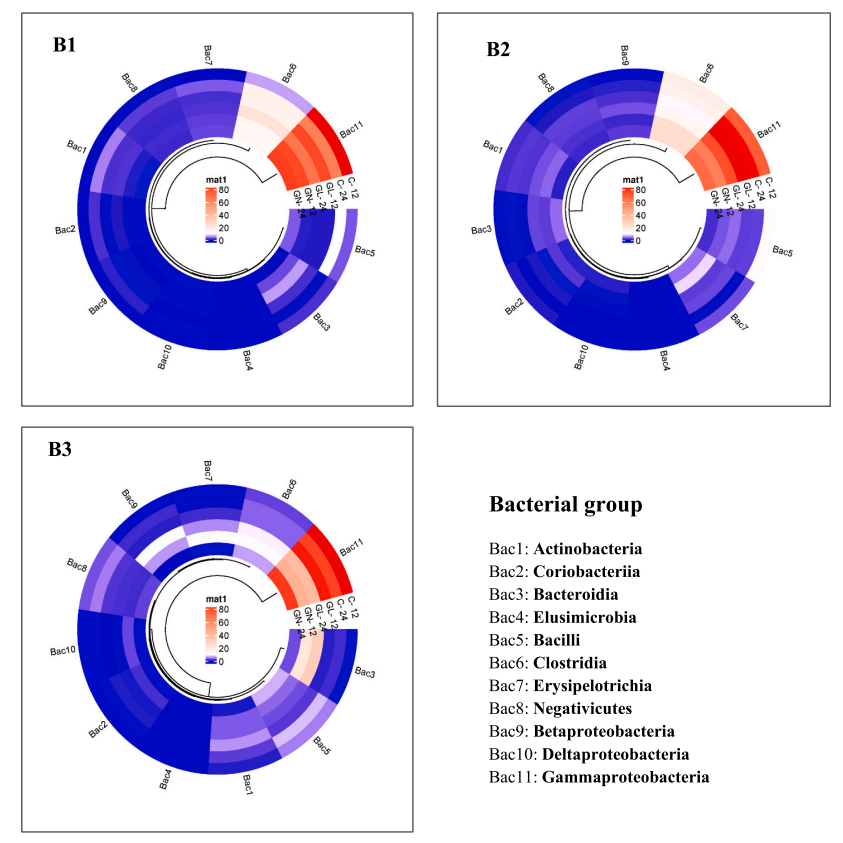
图5 细菌门类相对丰度(>0.01%)的圆形热图
注:C:对照组,灵芝提取物:GL,新日本灵芝提取物:GN,三个批次(B1、B2、B3)在发酵12小时和24小时时的情况
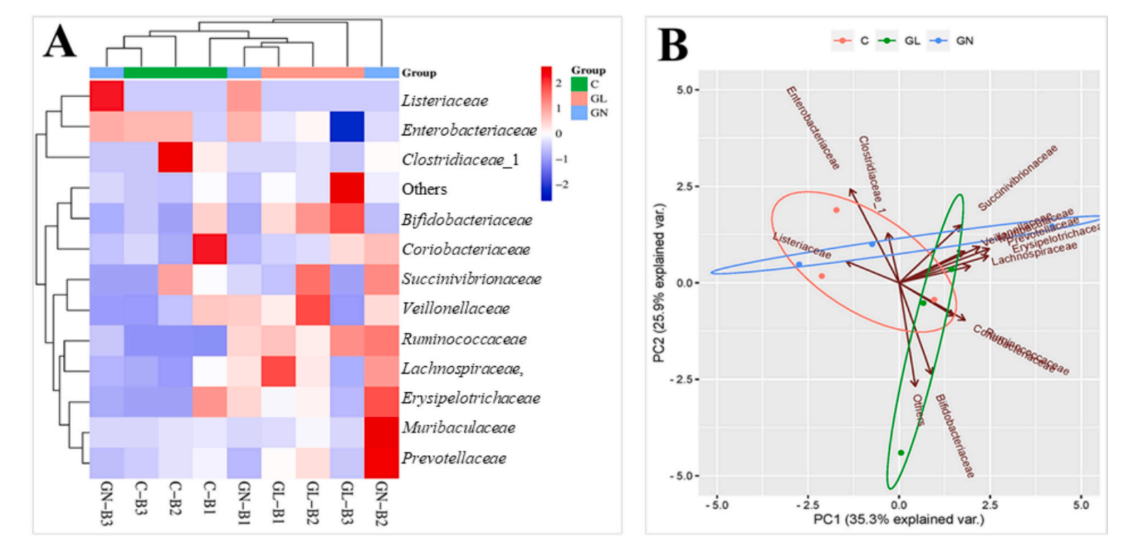
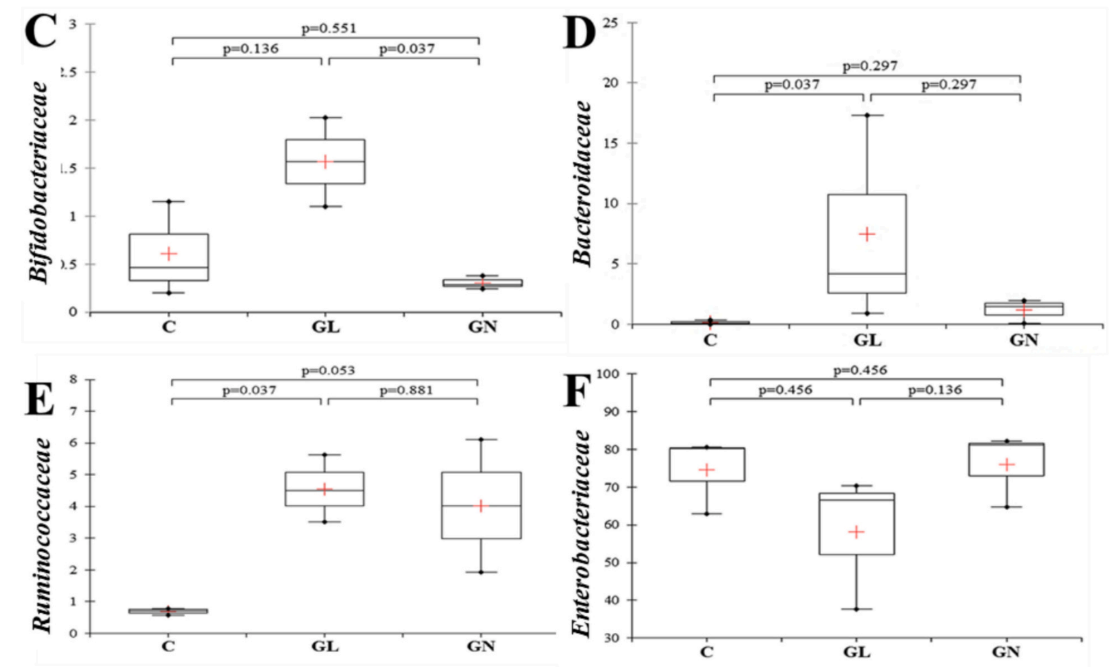
图6 细菌种群:科水平的群落组成
注:(A)标记的分类单元相对丰度>0.5%。“其他”表示相对丰度<0.5%;(B)细菌群落变化的主成分分析。组间细菌丰度的成对比较箱线图:双歧杆菌科(C)、拟杆菌科(D)、瘤胃球菌科(E)和肠杆菌科(F)。
三、对短链脂肪酸(SCFAs)产生的影响
GL和GN发酵均能显著提高SCFAs的产量,主要包括乙酸、丙酸和丁酸。不同批次中,GL和GN对 SCFAs 产量的影响存在差异,且GL发酵导致SCFAs增加的幅度在部分批次中大于 GN,表明GL可能更容易被肠道细菌利用。
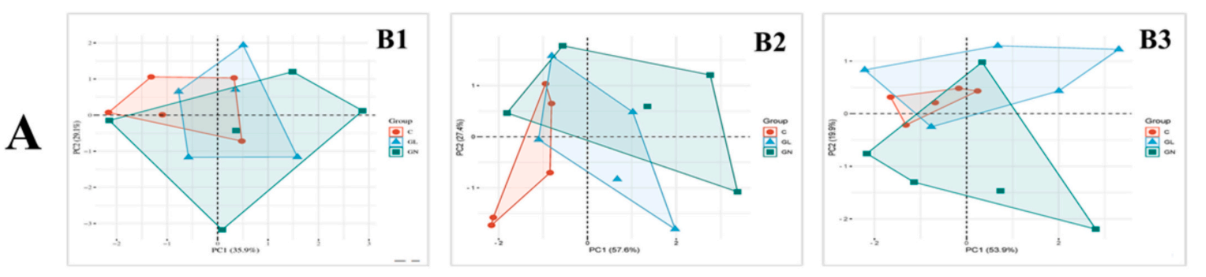

图7 发酵过程中短链脂肪酸含量(毫摩尔/毫升)的变化
注:(A)主成分分析(PCA)显示了各组之间总短链脂肪酸(SCFA)随时间的分布情况。每一批次中GL组和GN组短链脂肪酸增加的堆积柱状图:B1、B2、B3。LA:乳酸,AA:乙酸,PA:丙酸,BA:丁酸,IVA:异戊酸。
四、微生物群落与 SCFAs 的相关性
相关性分析显示,多种细菌科与 SCFAs 之间存在显著相关性。如乙酸、丙酸、丁酸等 SCFAs 水平的增加与肠杆菌科丰度的降低以及普雷沃氏菌科、瘤胃球菌科等有益菌科丰度的增加相关。
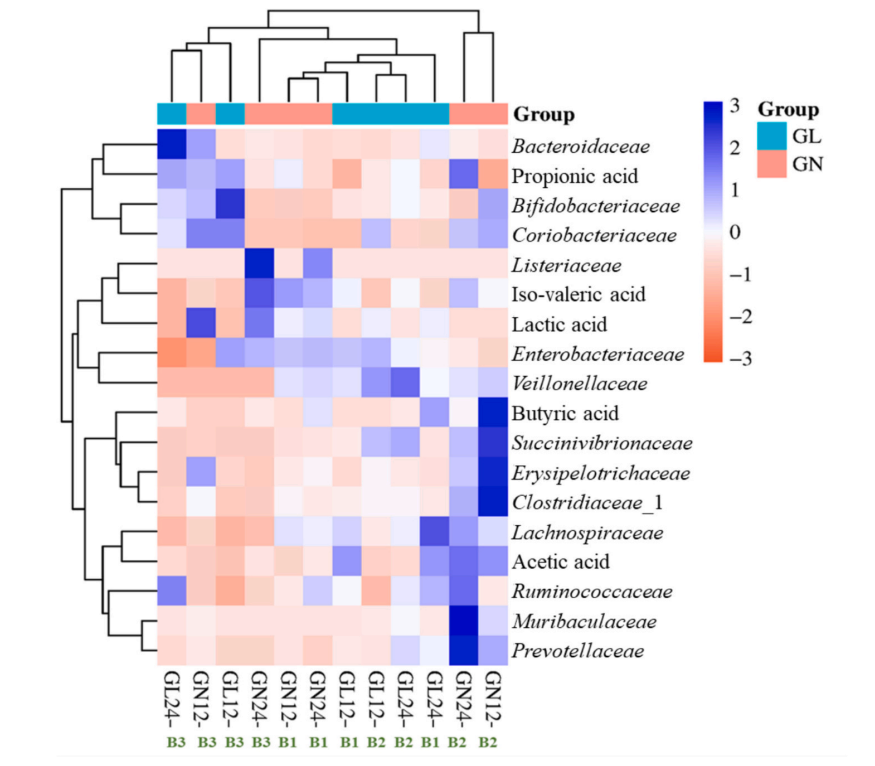
图8 基于欧几里得距离的热图,
注:GL组和GN组中三个批次(B1、B2和B3)的短链脂肪酸(SCFA)与细菌科之间的相关性
综上所述,GL和GN热水提取物主要由碳水化合物组成,同时含有大量蛋白质和酚类化合物。GL的蛋白质和总酚含量更高,两者单糖组成和结构存在差异。两种提取物均能被肠道菌群代谢,调节关键微生物类群的组成和丰度,抑制有害菌生长,促进有益菌增殖,且SCFAs增加的幅度表明GL的调节效果更明显。这些提取物通过调节肠道微生物群增加 SCFAs 的产生,可能对健康有益。然而,本研究存在局限性,如依赖体外模型、缺乏长期验证以及对生物利用度和活性化合物协同效应分析不足。未来研究应确定提取物中的具体活性化合物,阐明其调节肠道微生物群的机制,并开展体内研究验证其健康益处。
上一篇:来自金柄牛肝菌的新型甘露糖半乳糖聚糖的结构表征、功能特性和抗氧化潜力
下一篇:降糖新宠——羊肚菌多糖
1、凡本网所有原始/编译文章及图片、图表的版权均属微生物安全与健康网所有,未经授权,禁止转载,如需转载,请联系取得授权后转载。
2、凡本网未注明"信息来源:(微生物安全与健康网)"的信息,均来源于网络,转载的目的在于传递更多的信息,仅供网友学习参考使用并不代表本网同意观点和对真实性负责,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请速来函告知,我们将尽快处理。
3、转载请注明:文章转载自www.mbiosh.com
联系方式:020-87680942



